Debido a la pandemia por Coronavirus, de la noche a la mañana prácticamente toda la humanidad se ha visto en la necesidad de protegerse del contagio con Covid-19 negándole acceso al virus a la vía aérea, principal forma de contagio del mismo, sin embargo bien sea por desconocimiento o falta de acceso a los recursos adecuados, muchos no lo han hecho de la forma más adecuada.
En este sentido millones de personas han comenzado a usar tapabocas, respiradores, máscaras para gases, pañuelos e incluso bandanas como medios para «bloquear» al Covid-19 pero… ¿Son todos estos métodos efectivos?, ¿Hay alguna diferencia entre ellos?, ¿Quién debe usar qué?
Esas son solo algunas de las preguntas que vamos a responder a fin de ayudar a la población a tomar decisiones adecuadas con base en información científicamente probada.
En este punto es importante recalcar que el método de ensayo y error no tiene cabida en lo que a equipos de protección personal se refiere ya que el error por lo general termina siendo sinónimo de lesión o muerte, de allí que deban emplearse únicamente equipos de protección estudiados y probados científicamente a fin de contar con garantía de protección. Cualquier otro método podría terminar resultando tan solo utilería, dejando al usuario totalmente desprotegido.
Antes de comenzar es importante recordar algunos conceptos básicos que nos permitirán luego tratar el tema en profundidad, entre ellos la definición de métodos de barrera, equipos de protección personal y nivel de filtración.
Métodos de Barrera
Se conoce como método de barrera a aquellos métodos destinados a funcionar como un obstáculo en la vía de transmisión entre un enfermo y una persona sana. Estos métodos están pensados para uso a corto plazo y con exposición limitada ya que suelen verse superados en pocas horas por el agente contaminante o infeccioso contra el que pretenden combatir.
vía de transmisión entre un enfermo y una persona sana. Estos métodos están pensados para uso a corto plazo y con exposición limitada ya que suelen verse superados en pocas horas por el agente contaminante o infeccioso contra el que pretenden combatir.
Estos métodos no están diseñados para contener y aislar al enfermo o a la persona sana, simplemente dificultan la transmisión, eso quiere decir que de darse una exposición suficientemente larga e intensa, eventualmente habrá contagio; de allí que la Organización Mundial de la Salud (OMS) haya publicado recientemente que algunos métodos de barrera como los tapabocas pueden dar una «falsa sensación de seguridad».
Sin embargo el uso adecuado de estos métodos resulta clave para cortar la cadena de transmisión del coronavirus.
Equipos de Protección Personal
El siguiente nivel en bioseguridad son los equipos de protección personal. Se trata de dispositivos diseñados para aislar al individuo sano del enfermo en mayor o menor medida, de manera que mientras más alto el nivel de bioseguridad, más aislada queda la persona y por lo tanto más protegida.
Sin embargo hay que recordar que no existe un método que ofrezca 100% de seguridad y que la efectividad de los equipos de protección personal está íntimamente ligada a su uso adecuado, de manera que incluso el mejor de los equipos resultará inútil si no se usa de manera correcta.
Los equipos de protección personal en bioseguridad van desde el nivel 1 hasta el nivel 4, siendo uno de los más empleados durante la pandemia Covid-19 los respiradores con filtro.
Estos respiradores están diseñados para ofrecer distintos niveles de protección contra partículas de diversos tamaños, de allí que no todos son aptos para proteger al usuario del Covid-19.
Por lo general debido a la disponibilidad limitada y los altos costos, los equipos de protección personal se reservan para personal con exposición elevada a un agente infeccioso debido a las tareas que desempeña. En el caso particular del Covid-19 dicho material está siendo usado por médicos, personal de enfermería, bomberos y personal de seguridad en áreas de elevada exposición.
Nivel de Filtración
Cuando se habla del nivel de filtración se hace referencia a la capacidad de un material de retener partículas. Mientras más alto el nivel de filtración, más pequeñas las partículas que pueden retener, sin embargo hay que considerar que cuando se habla de partículas, en muchos casos se hace referencia a material microscópico, invisible al ojo humano, por lo que resulta imposible cuantificar a simple vista la capacidad de filtración de material, siendo para ello necesario el uso de instrumentos y métodos especializados de alta complejidad.
Tapabocas y Respiradores
Hablar de tapabocas y respiradores es hablar de un método de barrera y un equipo de protección personal y aunque a simple vista pueden resultar similares, la verdad es que funcionan de maneras muy distintas.
Los tapabocas o mascarillas quirúrgicas están diseñados para proteger la cara del usuario de partículas visibles o sub-visibles, siendo estas últimas aquellas que requieren una lupa para poder ser vistas. No llegan al nivel microscópico pero tampoco pueden ser identificadas a simple vista.
Por su parte los respiradores están diseñados para contener partículas en el orden de las micras (1 micra es igual a la milésima parte de 1 mm) por lo que el aire que ingresa a la vía respiratoria es mucho más limpio que el aire ambiente dado que la mayoría de las partículas (pero no todas y esto depende del nivel de filtración) son retenidas en los filtros del respirador.
Tapabocas o Mascarillas Quirúrgicas
Se trata de material médico de uso común en las emergencias, unidades de cuidado crítico y quirófanos de todo el mundo. Están diseñadas para limitar el intercambio de secreciones y material biológico entre el personal sanitario y los pacientes, ¡en ambos sentidos!, es decir, un tapabocas evita que el material biológico proveniente del paciente entre en contacto con la vía respiratoria del personal sanitario y a la vez evita que cualquier secreción de la vía respiratoria del personal alcance al paciente.
En este sentido es muy importante destacar que el tapabocas es una barrera y como tal tiene sus limitaciones. Normalmente están diseñados para contener material húmedo de manera que ayudan a evitar el contacto con gotas, microgotas y salpicaduras, sin embargo poseen poca o nula capacidad de filtración por lo que no ofrecen protección contra aerosoles y micropartículas en suspensión.
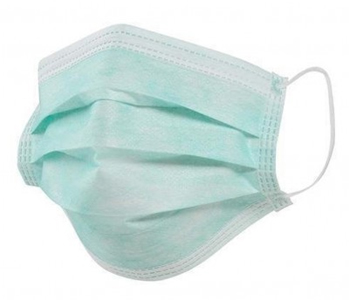 Por lo general los tapabocas están compuestos por tres capas de materiales diferentes. La parte más externa (la que se ve cuando está colocado) es material impermeable, de baja porosidad; a continuación existe una capa intermedia con cierta capacidad de filtrado (sobre todo para partículas del tamaño de un grano de polvo) y finalmente una capa interna (que tiene contacto con la piel del usuario) de material suave que permite cierto ajuste.
Por lo general los tapabocas están compuestos por tres capas de materiales diferentes. La parte más externa (la que se ve cuando está colocado) es material impermeable, de baja porosidad; a continuación existe una capa intermedia con cierta capacidad de filtrado (sobre todo para partículas del tamaño de un grano de polvo) y finalmente una capa interna (que tiene contacto con la piel del usuario) de material suave que permite cierto ajuste.
Los tapabocas pueden fijarse mediante bandas elásticas o tiras ajustables sin embargo ninguno de los dos métodos ofrece sello, es decir que el aire que ingresa a la vía respiratoria del usuario es aquel que pasa a través del tapabocas pero también el que ingresa a través de las zonas de ajuste laterales, superiores e inferiores donde la mascarilla ajusta en la piel pero sin generar sello.
Es importante destacar que cuando el material del tapabocas se humedece pierde su efectividad, de manera que al recibir una salpicadura o incluso estornudar con la mascarilla quirúrgica puesta, es necesario cambiarla de inmediato ya que de otro modo sería como no usar nada.
Considerando las características de diseño y limitaciones de las mascarillas quirúrgicas su utilidad en la prevención del Coronavirus se limita a:
1- Contener las gotas que expulsa una persona enferma al toser o estornudar
2- Limitar el ingreso a la vía aérea de las gotas que expulsa un enfermo o un portador sano al toser, estornudar o incluso hablar.
Para que una mascarilla quirúrgica proteja al usuario del coronavirus es indispensable que se den ciertas condiciones:
- La mascarilla no debe reutilizarse
- El tiempo de uso no debe exceder las recomendaciones del fabricante (por lo general 4 a 6 horas)
- Se deben sustituir inmediatamente si se humedecen
- No se deben emplear como equipo de protección en condiciones de alta exposición al virus (emergencias, salas de hospitalización, salas de aislamiento, etc)
En este punto es importante señalar que las mascarillas de tela, las artesanales y todo aquel sustituto de tapabocas (bandana, pañuelo, etc) NO OFRECE PROTECCIÓN contra el coronavirus, esto se debe principalmente a dos razones:
1- No se trata de material impermeable
2- Su nivel de filtración es escaso o nulo (hay que recordar que se habla de partículas microscópicas)
En este sentido es posible que algún tipo de tela sintética ofrezca algún tipo de protección, sin embargo considerando que no se cuenta con estudios de todos los materiales con los que se fabrican tapabocas caseros y de tela, no hay garantía de su efectividad, por lo tanto el usar este tipo de elemento de protección y no usar nada es prácticamente lo mismo.
En los casos donde la exposición sea sostenida o se trate de un entorno de alto riesgo NO ESTÁ INDICADO EL USO DE MASCARILLAS, en lugar de ello se deben emplear Respiradores.
Equipo de Protección Personal (EPP) – Respiradores
Los respiradores pueden parecer mascarillas a simple vista ya que cubren la nariz y la boca del usuario, sin embargo su diseño y la ingeniería detrás de los materiales con los que están fabricados estos EPP les confieren cualidades muy superiores a las de cualquier mascarilla quirúrgica.
En primer lugar los respiradores tienen un ajuste que permite un sello casi 100% impermeable entre la piel del usuario y el EPP de manera que todo el aire que ingresa a la vía respiratoria de este se ve forzado a pasar a través del material del respirador, específicamente a través de los filtros.
En general el respirador está fabricado con un material impermeable que ofrece una altísima resistencia al paso del aire por lo que su diseño es tal que el flujo de aire inspirado se ve forzado a pasar a través de  una serie de materiales porosos con alta capacidad de filtración, lo que elimina entre 95 y 99% de las partículas en el aire inspirado (según las características del EPP).
una serie de materiales porosos con alta capacidad de filtración, lo que elimina entre 95 y 99% de las partículas en el aire inspirado (según las características del EPP).
Así pues, los EPP limpian en gran medida el aire que respira el usuario, minimizando el riesgo de contagio por Covid-19, sin embargo como todo método mecánico, los EPP tienen sus limitaciones, muchas de ellas relacionadas con el uso inadecuado de los mismos.
Es por ello que el personal que utiliza este tipo de material debe estar debidamente entrenado en la manipulación, uso, ajuste y disposición final de los EPP ya que de otra forma no ofrecerían el nivel de protección para el cual están diseñados.
En este sentido hay que respetar las recomendaciones de cada uno de los fabricantes referentes al tiempo máximo de uso, exposición en ambientes con elevados niveles de humedad, manipulación y sello con la piel del usuario así como el tiempo de vida de los filtros en aquellos casos donde el EPP es reusable y solo se cambian los filtros.
La gama de EPP disponibles en el mercado es muy amplia, sin embargo los que se están con más frecuencia son los respiradores N95 o su equivalente (N95 es un código de fabricante que indica que el EPP filtra el 95% de las partículas presentes en el aire.
Es importante que el personal sanitario, de seguridad y todo aquel que se vea obligado a trabajar en entornos con elevado riesgo de contagio o exposición alta al coronavirus use de manera rutinaria y adecuada EPP tipo respirador, solo en conjunto con otras medidas de protección de bioseguridad a fin de minimizar las posibilidades de contagio.
En cuanto a la población general, el uso del tapaboca es suficiente siempre teniendo en cuenta que debe limitarse su uso y la exposición, eso quiere decir que el hecho de usar el tapabocas no nos ofrece protección alguna si nos exponemos por horas y horas en la calle, entramos a sitios con aglomeraciones o ingresamos a áreas donde se encuentran personas enfermas, siendo en este último caso necesario usar equipos de protección personal.




 vía de transmisión entre un enfermo y una persona sana. Estos métodos están pensados para uso a corto plazo y con exposición limitada ya que suelen verse superados en pocas horas por el agente contaminante o infeccioso contra el que pretenden combatir.
vía de transmisión entre un enfermo y una persona sana. Estos métodos están pensados para uso a corto plazo y con exposición limitada ya que suelen verse superados en pocas horas por el agente contaminante o infeccioso contra el que pretenden combatir. Por lo general los tapabocas están compuestos por tres capas de materiales diferentes. La parte más externa (la que se ve cuando está colocado) es material impermeable, de baja porosidad; a continuación existe una capa intermedia con cierta capacidad de filtrado (sobre todo para partículas del tamaño de un grano de polvo) y finalmente una capa interna (que tiene contacto con la piel del usuario) de material suave que permite cierto ajuste.
Por lo general los tapabocas están compuestos por tres capas de materiales diferentes. La parte más externa (la que se ve cuando está colocado) es material impermeable, de baja porosidad; a continuación existe una capa intermedia con cierta capacidad de filtrado (sobre todo para partículas del tamaño de un grano de polvo) y finalmente una capa interna (que tiene contacto con la piel del usuario) de material suave que permite cierto ajuste. una serie de materiales porosos con alta capacidad de filtración, lo que elimina entre 95 y 99% de las partículas en el aire inspirado (según las características del EPP).
una serie de materiales porosos con alta capacidad de filtración, lo que elimina entre 95 y 99% de las partículas en el aire inspirado (según las características del EPP).
 tipo de estudio cardíaco más complejo.
tipo de estudio cardíaco más complejo.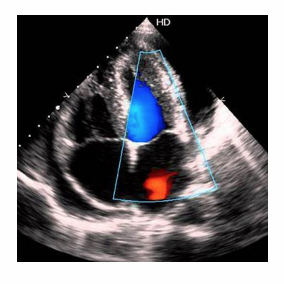 paciente por vía endovenosa un fármaco conocido como dobutamina cuyo efecto es acelerar la frecuencia cardíaca y elevar la tensión arterial, simulando así los cambios hemodinámicos presentes en el ejercicio.
paciente por vía endovenosa un fármaco conocido como dobutamina cuyo efecto es acelerar la frecuencia cardíaca y elevar la tensión arterial, simulando así los cambios hemodinámicos presentes en el ejercicio.
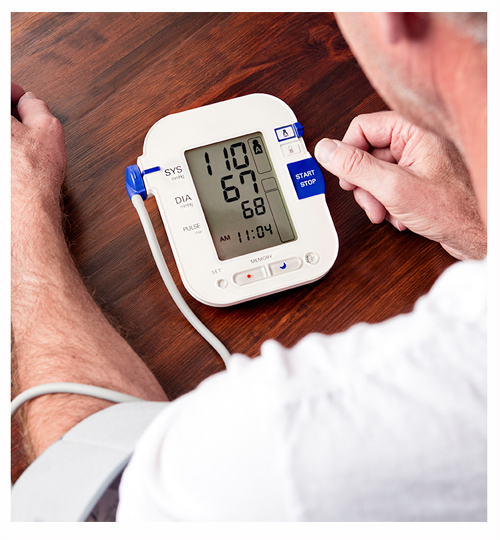 salud pública de alcance global (se calcula que entre 20 y 30% de la población mundial sufre algún grado de hipertensión) sino que además el control de las cifras de tensión arterial dentro de niveles adecuados resulta crítica para la buena salud cardiovascular.
salud pública de alcance global (se calcula que entre 20 y 30% de la población mundial sufre algún grado de hipertensión) sino que además el control de las cifras de tensión arterial dentro de niveles adecuados resulta crítica para la buena salud cardiovascular.